Heparine
- Unfraktioniertes Heparin
- Niedermolekulares Heparin
- Fachinformationen unter http://www.fachinfo.de
Unfraktioniertes Heparin
Z.B. Calciparin®, Liquemin® N, Thrombophob®.
Amp. (1 ml) à 5000 IE/7500 IE/10 000 IE/20 000 IE.
Wirkmechanismus
- Bei niedriger Dosierung verstärkt Heparin im Komplex mit AT III die AT-III-Wirkung um das 7 bis 8-fache. Bei hoher Dosierung werden die Faktoren IXa, Xa, XIa, XIIa inaktiviert. Außerdem wird die Thrombinwirkung aufgehoben und die Plättchenaggregation gehemmt. Erhöhte Freisetzung einer Lipoproteinlipase mit Abbau von Chylomikronen, Beschleunigung des Histaminabbaus, Reduktion der Aldosteronbildung.
- Gemisch aus sulfatierten Mukopolysacchariden mit unterschiedlichen MG von 3000–50000.
- Pharmakokinetik: Nur parenterale Gabe (s.c., i.v.), Bioverfügbarkeit 15–30 %, Verteilungsvolumen ca. 0,05 l/kg (Intravasalraum), Plasmaproteinbindung 95 %. Elimination (Clearance) nach i.v.-Bolus rasch durch Bindung v.a. an histidinreiche Glykoproteine und Plättchenfaktor 4 und Metabolisation durch Makrophagen und Endothelzellen. Besonders bei hohen Dosen nach Absättigung der bindenden Proteine langsamere renale Ausscheidung. HWZ: 30 Min. (i.v.-Bolus mit 25 IE/kg), 60 Min. (i.v.-Bolus mit 100 IE/kg). D.h. ein full-dose Heparin-Bolus bietet thromboembolischen Schutz für ca. (3-)4 h.
Indikationen
- Thromboseprophylaxe (low dose).
- Frischer Myokardinfarkt zur Prophylaxe der Thrombenbildung im hypokinetischen Infarktareal und in den Koronararterien.
- Vollheparinisierung bei arteriellen oder venösen Verschlüssen (Embolien, Thrombosen), Kardiomyopathie, Mitralinsuff. bei gleichzeitiger absoluter Arrhythmie, künstlicher Herzklappe vor und parallel zur beginnenden Marcumarisierung bzw. perioperativ, bei zentralen Embolien und protrahiertem zerebralem Insult nach Ausschluss eines hämorrhagischen Infarkts.
- Anschlussbehandlung nach Ther. mit Streptokinase und APSAC sowie in Kombination mit Urokinase und Alteplase bei Lyse.
- Dialysebehandlung, AV-Filter, extrakorporaler Blutfluss.
- Initialther. (5000 IE i.v.) sowie Anschlussbehandlung nach lokaler Lysebehandlung einer Basilaristhrombose.
- Verbrauchskoagulopathie (low dose: 400–600 IE/h).
- Bei neu aufgetretenem Vorhofflattern bzw. Vorhofflimmern vor Rhythmisierung.
Dosierung
- Low dose: 200 IE/kg/d (10000 IE auf 50 ml NaCl 0,9 %; 3 ml/h = 600 IE/h bei 70 kg).
- Vollheparinisierung/high dose: 400 IE/kg/d Bolusgabe von 5000 IE i.v., anschließend Perfusor mit 10000 IE auf 50 ml NaCl 0,9 % mit 5–7 ml/h = 1000–1400 IE/h unter aPTT-Kontrolle (Verlängerung der aPTT auf das 1,5 bis 2-fache des Ausgangswerts angestrebt).
Nebenwirkungen
- Blutungsgefahr bei Überdosierung bzw. Begleiterkrankung mit Störung des Gerinnungssystems.
- Thrombopenie, HIT-Sy.
- Selten allergische Reaktionen.
- Anstieg von Cholesterin und Triglyceriden im Plasma, Transaminasen, γ-GT.
- Haarausfall (gering, reversibel), Osteoporose (bei Langzeitther. > 20000 IE/d).
- Großflächige erythematöse Infiltrate mit Schmerzen an den Einstichstellen, Ekzeme, Heparinnekrose.
Wechselwirkung
- Verstärkte Blutungsgefahr durch Thrombozytenaggregationshemmer und Dextrane.
- Antihistaminika, Digitalispräparate und Tetrazykline hemmen partiell die Heparinwirkung.
Cave
- Heparine (fraktionierte und unfraktionierte) benötigen zur vollen Entfaltung ihrer Antikoagulationswirkung normale AT-III-Spiegel. Bei extrem niedrigen AT-III-Spiegeln ist keine oder nur eine eingeschränkte Antikoagulation zu erreichen.
- Dosisanpassung nach aPTT, v.a. bei Leberinsuff., Thrombopenie.
- Bei terminaler Niereninsuff. Dosisreduktion der High-dose-Heparinisierung um ca. 25 %.
- Bei Allergie Wechsel des Präparats, da Allergie gegen Zusatzstoffe möglich ist, evtl. niedermolekulares Heparin.
- In der Schwangerschaft anwendbar.
- Antidot: Protaminchlorid (Protamin® ICN), 1000 IE Protamin neutralisieren 1000 IE Heparin. Ist die Antagonisierung innerhalb weniger Min. nach i.v.-Injektion nötig: 100 %-Dosis geben, 60 Min. nach i.v. Injektion: 50 %-Dosis, 120 Min. nach i.v.-Injektion: 25 %-Dosis geben.
- Bei s.c.-Heparininjektion Protaminsulfat (Protaminsulfat Leo®) in einer Dosis geben, die 50 % der letzten Heparindosis antagonisiert.
![]()
Nachteile von Unfraktionierten Heparinen
- kurze Halbwertszeit (kann auch ein Vorteil sein)
- Bioverfügbarkeit bei s.c. Injektion nur ca. 15-30 %
- mehrmals tägliche Injektionen
- mangelhafte Dosis-Wirkungs-Beziehung:
- die Pharmakokinetik von UFH ist dosisabhängig
- gerinnungshemmender Effekt ist von Patient zu Patient erheblichen Schwankungen unterworfen (bis zur vollständigen Resistenz)
- bei Langzeitanwendungen wurde steigendes Osteoporoserisiko beobachtet
- Heparin-induzierte Thrombozytopenie vom Typ II
![]()
Niedermolekulares Heparin
Wirkmechanismus von Heparin
- Heparine sind heterogene Stoffgemische aus Schweinedarm-Mucosa.
- Antithrombin (Co-Faktor) zur Gerinnungshemmung nötig, nur 1/3 der Heparin-Moleküle ist wirksam – 2/3 sind »unspezifisches Material«.
- Heparin/Antithrombin-Komplex inhibiert Thrombin (Faktor IIa) und Faktor Xa.
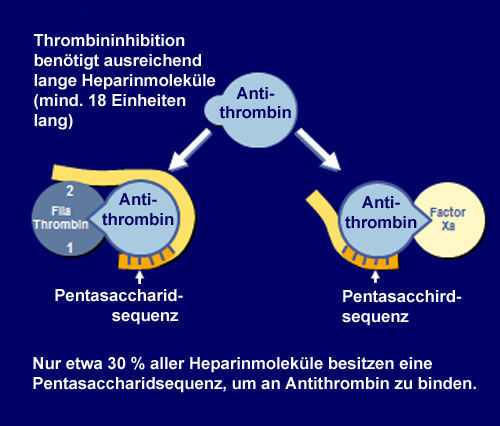
Abb. 11.1: Wirkung der Heparine auf Thrombin und Faktor Xa.
Verhältnis Hemmung FIIa : FXa
Unfraktioniertes Heparin (UFH) 1 : 1
Niedermolekulares Heparin (NMH) 1 : 2,5–4.
Wirkmechanismus
- Heparinpräparate, die durch Depolymerisation auf ein MG von 4000–9000 Dalton eingeengt wurden. Hemmung des F Xa und des Prothrombins im Verhältnis 2–3:1 je nach Präparat durch Fehlen der höhermolekularen Anteile des Heparingemisches. Geringerer Bindungsgrad an verschiedene Proteine und Zellen als bei unfraktionierten Heparinen, dadurch bessere Bioverfügbarkeit und eher voraussagbare Dosis-Wirkungs-Beziehung.
- Pharmakokinetik: Bioverfügbarkeit 95 %. Clearance überwiegend renal. HWZ nach i.v.-Gabe 2–3 h, nach s.c.-Gabe durch langsame Freisetzung aus dem Gewebedepot mehr als 18 h, so dass die Gabe 1 ×/d in der low-dose-Ther. möglich ist. Peak-Werte unabhängig von der Dosis nach 3–4 h.
Indikationen
- Wie unfraktioniertes Heparin.
- Thrombopenie, Unverträglichkeit und Allergie nach Heparingabe.
Dosierung
- Bei s.c. Applikation je nach gewünschter Antikoagulationsstärke Gabe von:
- 1 × niedrigste verfügbare Dosis pro d (Prophylaxe bei niedrigem Risiko), z. B. Clexane 20®.
- 1 × zweitniedrigste Dosis (z. B. Fragmin P forte®) oder 2 × niedrigste Dosis/d bei mittlerem Risiko.
- 2 × zweitniedrigste Dosis bei höherem Risiko.
- Bis maximal 200 IE/kg KG, auf 1 oder max. 2 Dosen/d verteilt bis max. 20 000 IE/d (aus Multidose-Packungen).
- Monitoring der Anti-Xa-Aktivität ist i.d.R. nicht notwendig.
- Bei s.c.-Applikation körpergewichtsangepasste Gabe von 200 IE/kg KG/d in 1 oder auch 2 Dosen (alle 12 h). Keine Steuerung über aPTT möglich. Evtl. Messung der Anti-Xa-Aktivität (selten indiziert). Therapiebereiche: 0,2–0,4 anti-Xa-U/ml (low dose), 0,5–1,2 anti-Xa-U/ml (high dose).
Nebenwirkungen
- HIT II, aber deutlich seltener als bei UFH.
- Blutungsgefahr bei Überdosierung bzw. Begleiterkrankung mit Störung des Gerinnungssystems, Niereninsuff.
- Selten allergische Reaktionen (mögliche Symptome: Fieber, Urtikaria, Exanthem, Konjunktivitis, Asthma, Anaphylaxie), auch gegen einzelne Präparate.
- Thrombopenie.
- Haarausfall (gering, reversibel), Osteoporose (bei Langzeitther. > 20000 IE/d, aber seltener als bei UFH).
- Großflächige erythematöse Infiltrate mit Schmerzen an den Einstichstellen, Ekzeme, Heparinnekrose.
- Anstieg von Cholesterin und Triglyceriden im Plasma.
- Häufiger reversibler Anstieg von GOT, GPT, γ-GT, LDH, Lipase im Serum. Seltener Anstieg von Kalium.
Kontraindikationen
HIT II, da häufig Kreuzreaktion der HIT-II-AK auch gegen niedermolekulare Heparine.
Wechselwirkung
- Thrombozytenaggregationshemmer, Cumarin (verstärkte Blutungsgefahr).
- Dextrane (verstärken Blutungsgefahr).
- Wirkungsverstärkung bei hochdosierter Ther. mit Penicillin oder Cephalosporin, nichtsteroidalen Antiphlogistika.
- Wirkungsverstärkung von Propranolol.
- Antihistaminika, Digitalispräparate und Tetrazykline hemmen partiell die Heparinwirkung, Wirkungsabschwächung durch Nitroglycerin i.v.
Cave
- Das Antidot Protaminchlorid (Protamin ICN®) antagonisiert niedermolekulare Heparine nur zu ca. 30-70 %. Die Antikoagulationswirkung kann daher nur teilweise gehemmt werden.
- Keine i.m.-Spritzen insbes. bei High-dose-Ther.
- Heparininduzierte Thrombopenie auch nach Gabe von niedermolekularem Heparin möglich!
![]()
Vorteile von Niedermolekularen Heparinen (LMH) vs. unfraktioniertem Heparin (UFH)
- geringere Tendenz, unspezifisch an Proteine und Zellen zu binden als UFH
- Interaktionen mit Thrombozyten schwächer ! = werden nicht durch PF-4 neutralisiert
- viel seltener Induktion einer HIT-II !!
- Halbwertszeit ca. doppelt so lange wie UFH
- Halbwertszeit nicht dosis– sondern substanzabhängig
- nach s.c. Injektion fast vollständig bioverfügbar
- ausschließlich renale Elimination (!!)
- konstante Dosis-Wirkungs-Beziehung, i.d.R. keine Laborkontrollen nötig
![]()
Tab. 11.2: Vergleich von unfraktioniertem (UFH) und niedermolekularem Heparin (NMH)
| Eigenschaft | UFH | NMH |
| Mittleres Molekulargewicht | 15.000 Da | 5.000 Da |
| Bioverfügbarkeit s.c. | 15-30 % | 85-95 % |
| Halbwertszeit - nach i.v.-Gabe - nach s.c.-Gabe |
1 h 2 h |
2 h 3-4 h |
| Anti-IIa-(Thrombin-)Aktivität | stark | schwach |
| Anti-Xa-Aktivität | schwach | stark |
| Bindung an Proteine | stark | schwach |
| Interaktion mit Thrombozyten | stark | schwach |
| Neutralisation durch Plättchenfaktor 4 | ja | nein |
| Induktion von HIT-Typ II | stark | schwach |
| Osteoporoserisiko | ja | reduziert |
| Elimination | RES, renal | renal |
| Dosis-Wirkungs-Beziehung | hoch, variabel | konstant |
| Monitoring | erforderlich | nicht erforderlich * |
| Neutralisation mit Protamin | 100 % | 40-60 % |
| Produktäquivalenz | ja | nein |
s.c.: subkutan, i.v.: intravenös,
HIT: heparininduzierte Thrombozytopenie, RES: retikuloendotheliales System.
* Ausnahmen bei Niereninsuffizienz, mechanischem Herzklappenersatz, Schwangerschaft.
![]()
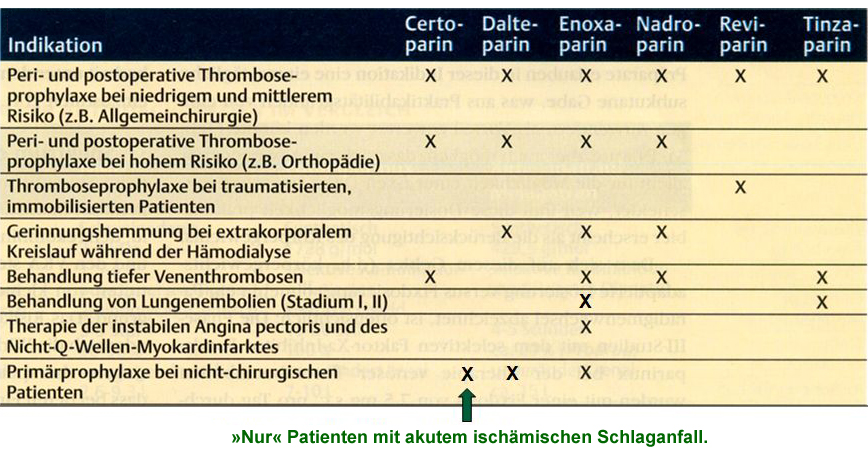
Tab. 11.3: Indikationsabhängiger Zulassungsstatus für verschiedene Niedermolekulare Heparine (NMH) in Deutschland